연구 배경
논문에 소개된 면역소재는 표고버섯 균사체(Lentinus edodes)와 쌀겨를 생물공정으로 처리해 얻은 물질로, 이후 헤미셀란으로 명명되었습니다.
본 연구에서는 이 물질이 병원성 살모넬라 감염 상황에서 면역세포의 항균 기능을 어떻게 조절하는지를 분석했습니다.
헤미셀란은 자가포식을 유도한다
논문에서 가장 명확하게 확인된 결과는 다음과 같습니다.
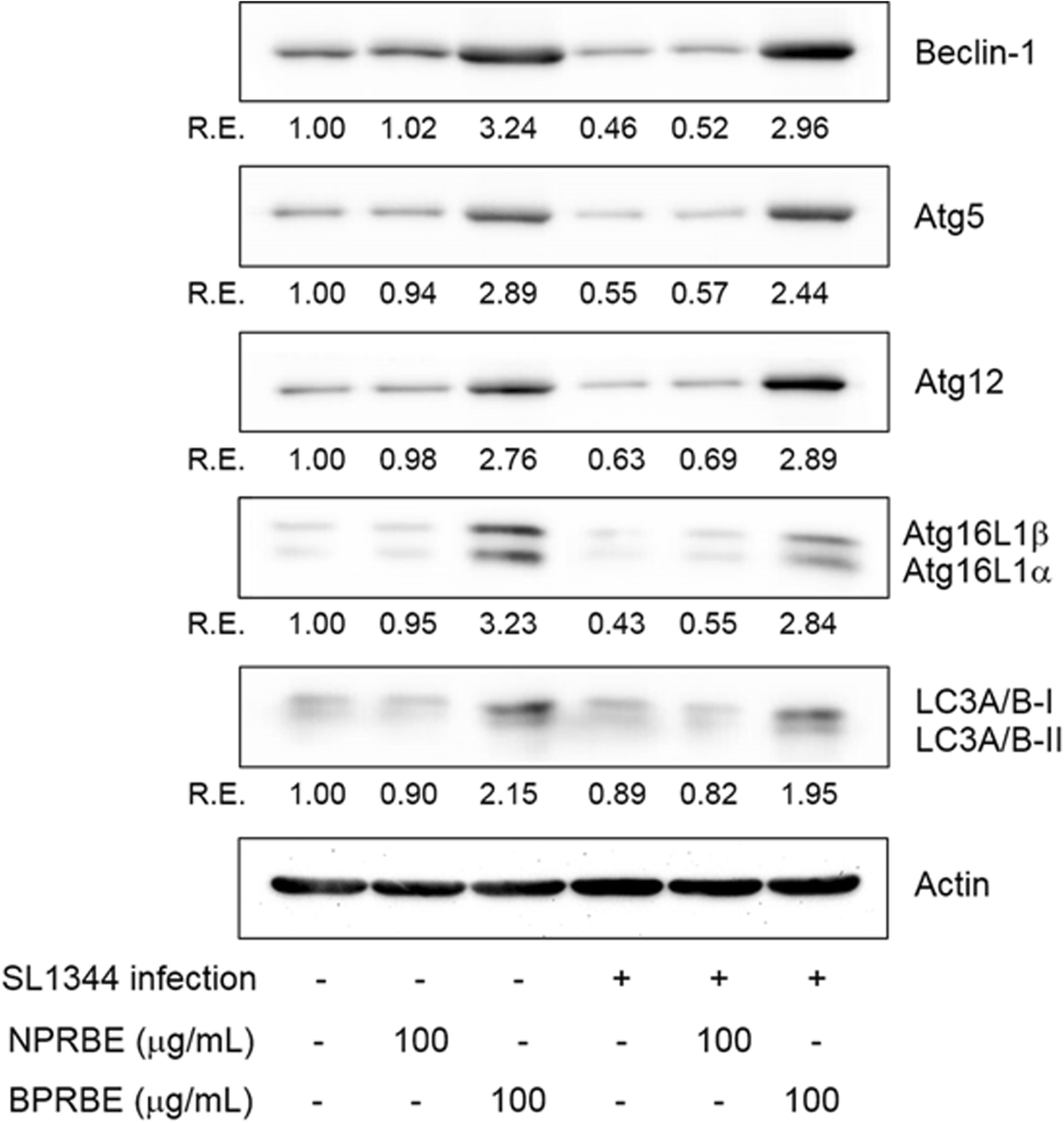
살모넬라에 감염된 대식세포에서는 일반적으로 자가포식 관련 단백질 발현이 감소하며, 이 때문에 살모넬라가 대식세포 안에서 생존할 수 있습니다.
그러나 헤미셀란을 처리한 경우, 이러한 억제가 해제되며 자가포식 관련 지표들이 유의하게 증가했습니다.
관찰된 변화는 Beclin-1 발현 증가, Atg5·Atg12·Atg16L 발현 증가, LC3-I에서 LC3-II로의 전환 증가로 요약됩니다. 이 결과는 헤미셀란이 대식세포에서 자가포식 기전을 활성화한다는 직접적인 실험적 근거에 해당합니다.
자가포식은 세균 제거와 연결된다
자가포식이 활성화되면서 대식세포 내 살모넬라의 자가용해소체(autolysosome) 포획이 증가했고, 세포 내 세균 생존율은 감소했으며, 생쥐 모델에서는 내부 장기로의 세균 전이도 줄었습니다. 이는 자가포식 유도가 세포 자율적 항균 작용(cell-autonomous bactericidal activity)으로 이어진다는 점을 보여줍니다.
TRIF–IFN-β–자가포식 경로의 개연성
자가포식 활성화와 더불어 논문에서는 IRF-3 인산화 증가와 인터페론 베타(IFN-β) 분비 증가도 함께 보고했습니다. 이 두 지표는 TRIF 의존적 신호 전달 경로 활성화의 전형적인 결과입니다.
또한 자가포식에 의해 생성된 세균 분해 산물이 엔도좀 수용체를 자극해
TRIF–IRF-3–IFN-β 경로를 활성화한다는 점은 기존 면역학 연구들과 일관됩니다.
따라서 본 연구 결과를 종합하면 다음과 같이 해석할 수 있습니다.
헤미셀란은
대식세포에서 자가포식을 유도하며,
그 작동 경로는 TRIF–IFN-β–자가포식 축일 가능성이 높다.
본 논문은 이 경로를 직접 차단 실험으로 증명하지는 않았지만,
자가포식 활성화와 TRIF–IFN-β 반응이 동시에 관찰되었다는 점에서 충분한 개연성을 제시합니다.
정리
본 연구를 종합하면, 헤미셀란은 대식세포에서 자가포식을 유도하고 이 활성은 세포 내 살모넬라 제거로 이어집니다. 또한 IRF-3 활성화와 IFN-β 증가를 고려할 때 해당 효과는 TRIF–IFN-β–자가포식 경로를 통해 매개될 가능성이 높습니다. 이는 헤미셀란이 직접적인 살균 물질이라기보다 면역 반응을 조절하는 물질임을 보여주는 중요한 근거입니다.
참고문헌
-
Kim SP, et al. Bioprocessed rice bran extract enhances autophagic capture of Salmonella in macrophages. BMC Complementary and Alternative Medicine. 2018. DOI | 저널 원문
-
Owen KA, et al. TRIF-dependent type I interferon responses in macrophages. mBio. 2016. DOI | 저널 원문
-
Wang L, et al. Autophagy and ubiquitination in Salmonella infection. Frontiers in Cellular and Infection Microbiology. 2018. DOI | 저널 원문
• • •